Le métabolisme - Chaîne respiratoire (1)
Phosphorylation oxydative
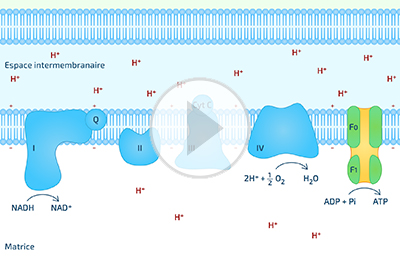
La chaîne respiratoire est localisée dans la membrane interne mitochondriale. Cette chaîne de transport d'électrons est constituée de quatre complexes protéiques :
- complexe I : NADH-coenzyme Q oxydoréductase,
- complexe II : succinate-coenzyme Q oxydoréductase,
- complexe III : coenzyme Q-cytochrome c oxydoréductase,
- complexe IV : cytochrome c oxydase.
Le coenzyme Q (ubiquinone) et le cytochrome c sont des transporteurs mobiles de la chaîne respiratoire.
Une grande partie de l'énergie produite dans les voies cataboliques se retrouve contenue dans le NADH et le FADH2 ; elle sera convertie en ATP dans la mitochondrie : les coenzymes réduits mitochondriaux cèdent leurs deux électrons à un système de transporteurs qui, par une cascade de réactions d'oxydo-réduction, amène ces électrons jusqu'à l'accepteur final, l'oxygène moléculaire. La membrane interne est imperméable aux ions H+, cependant, au cours de ce transfert électronique, il y a formation d'un gradient de protons de part et d'autre de cette membrane, ce qui permet la synthèse d'ATP lors d'une réaction catalysée par l'ATP synthase mitochondriale. La respiration et la phosphorylation de l'ADP sont donc couplées via ce gradient de protons.
Cette animation présente une version simplifiée du flux d'électrons accompagné du transfert de protons à travers la membrane interne mitochondriale.
Le NADH, formé dans la matrice, cède ses équivalents réducteurs à la NADH déshydogénase (complexe I), accessible par la face interne de la membrane interne. Ces électrons vont cheminer du complexe I jusqu'à l'oxygène moléculaire, via les coenzyme Q - complexe III - cytochrome c - complexe IV. L'oxygène moléculaire, accepteur final des électrons, sera réduit en H2O selon la réaction ½ O2 + 2 H+ + 2 e- à H2O.
Le FADH2 produit dans la matrice mitochondriale (non représenté sur l'animation) cède, quant à lui, ses équivalents réducteurs au complexe II. Le cheminement des électrons est ensuite identique à celui suivi par les électrons fournis par le NADH (coenzyme Q - complexe III - cytochrome c - complexe IV).
Au cours de ce transfert, des protons sont expulsés de la matrice vers l'espace intermembranaire (au niveau des complexes I, III et IV) ce qui crée, de part et d'autre de la membrane interne, un gradient électrochimique d'ions H+ qui contient l'énergie d'oxydation. Il est constitué d'un gradient de pH (la matrice devient plus basique) et d'un gradient de charges (la face matricielle de la membrane interne est chargée négativement).
Le retour des protons dans la matrice se produit au niveau de passages spécifiques constitués par l'ATP synthase (complexes FoF1) : Fo est un canal transmembranaire qui laisse passer sélectivement les protons, F1 contient le site catalytique responsable de la synthèse de l'ATP à partir d'ADP et de Pi. Le gradient électrochimique de protons fournit ainsi l'énergie nécessaire à la synthèse d'ATP, on dit qu'il est déchargé : 3 protons sont nécessaires à la synthèse d’un ATP.